解读《药品召回管理办法(征求意见稿)》的八个变化
发布时间:2020-10-20
文 | 郭亚飞 合伙人 边不拘 汇业律师事务所
我国目前现行有效的《药品召回管理办法》(下称:现行管理办法)发布于2007年12月10日,已明显不符合现行《药品管理法》、《疫苗管理法》的相关要求,国家药监局官网于2020年10月13日发布了《药品召回管理办法(征求意见稿)》(下称:征求意见稿),在原规定基础上进行了较大幅度的调整。笔者本文通过一张要点列表、两张流程简图、八点变化说明对这份征求意见稿进行全方位梳理和解读,力求帮助药企快速了解调整后的药品召回制度。
一、征求意见稿要点梳理列表
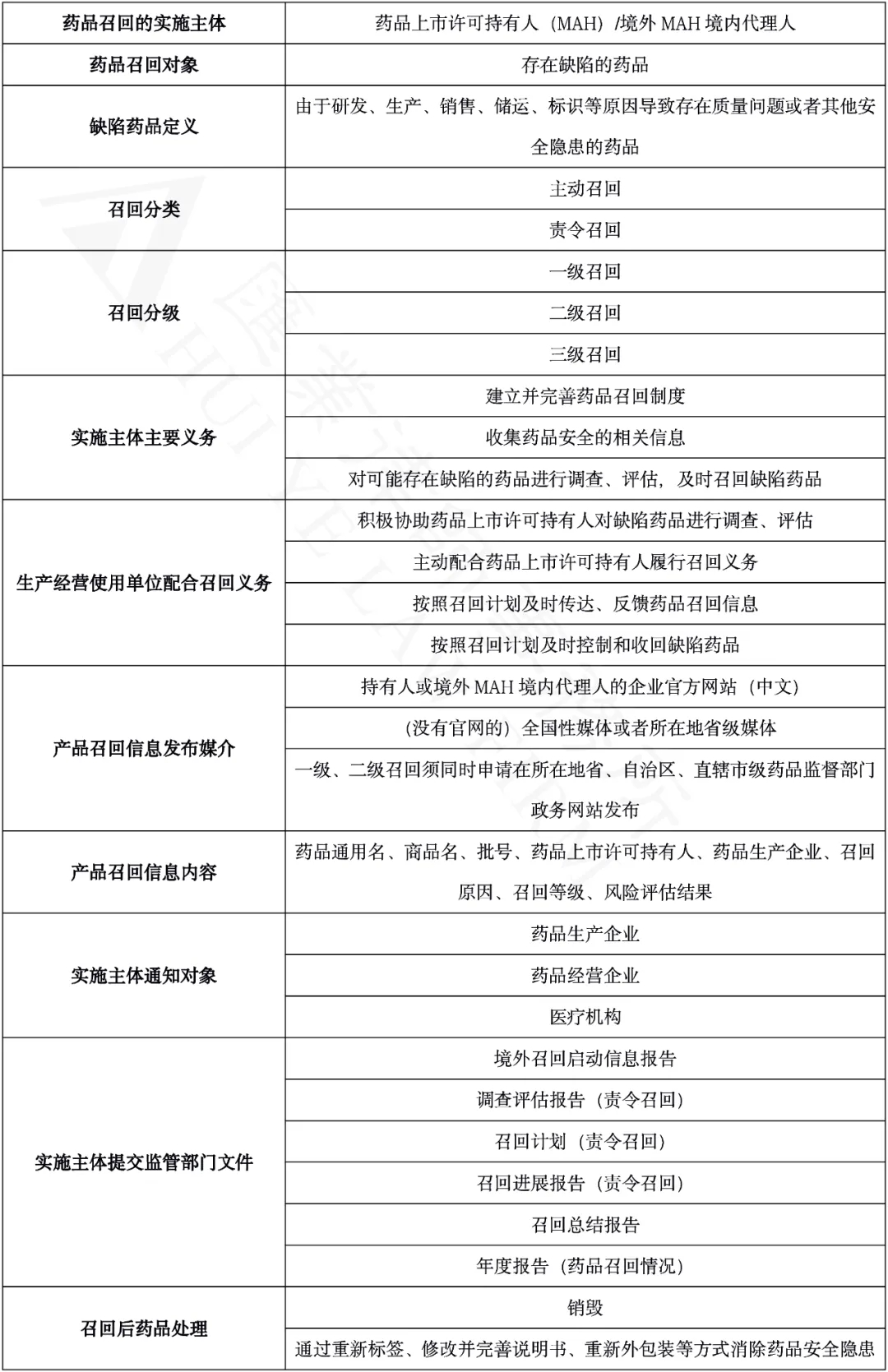
二、两个召回流程——主动召回与责令召回
1.主动召回流程图
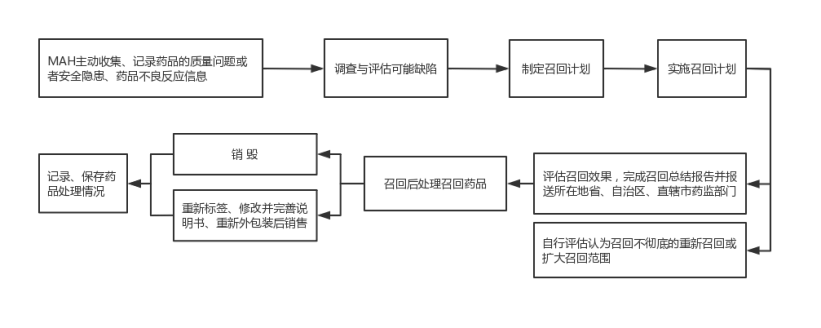
2.责令召回流程流程图
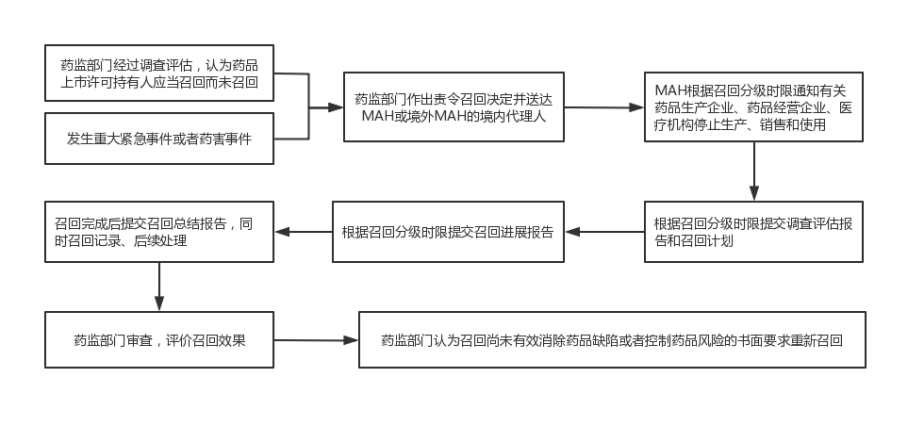
三、八个变化要点
1.召回实施主体与召回对象的变化
征求意见稿已将现行办法中的药品召回实施主体由“药品生产企业”改为“药品上市许可持有人”,召回对象由“存在安全隐患的药品”改为“存在缺陷的药品”,并明确了“缺陷药品”的定义。首先,上述修改落实了《药品管理法》以药品上市许可持有人为主线的管理体系;其次,为最大程度保护患者的健康权益并明晰药品上市许可持有人责任,征求意见稿将召回对象的范围也予以扩大和细化,药品上市许可持有人不仅要关注现行管理办法中规定的研发、生产环节,还须关注销售、储运环节以及标识问题,体现了对药品上市许可持有人药品全生命周期的责任要求。对召回对象的这一修改也与2017年《医疗器械召回管理办法》中的表述保持了一致。
2.进口药品境内召回实施主体及报告对象的变化
征求意见稿将进口药品境内召回的实施主体由“进口单位”全部集中归口到“境外药品上市许可持有人指定的在中国境内的企业法人”,并依据《药品管理法》在药品召回上与“境外药品上市许可持有人”承担连带责任,改变了对原“进口单位”未履行药品召回责任进行处罚却无法可依的情况。
征求意见稿进一步将召回信息报告对象由“国家食品药品监督管理局”改为“中国境内企业法人所在地的省、自治区、直辖市药品监督管理部门”进行属地管辖,下放事权,理顺行政管理关系。
3.增加了将召回信息纳入年度报告的要求
因为《药品管理法》第三十七条规定:“药品上市许可持有人应当建立年度报告制度,每年将药品生产销售、上市后研究、风险管理等情况按照规定向省、自治区、直辖市人民政府药品监督管理部门报告。”药品召回信息属于风险管理范畴,因此被纳入年度报告的内容。
4.召回责任主体及配合单位相关义务的变化
征求意见稿明确了药品上市许可持有人是控制与消除药品缺陷的责任主体,对其保留了现行管理办法中原规定在“药品生产企业”名下的义务。在生产经营使用单位配合召回义务中增加了“应当积极协助药品上市许可持有人对缺陷药品进行调查、评估”的内容;保留了原有的其他义务表述。笔者认为此处仍会给持有人造成疑惑的是,上市许可持有人在实务操作中是否有义务自行“控制和收回缺陷药品”,还是履行到通知配合单位即可。鉴于研制机构也可成为药品上市许可持有人,而研制机构一般不具有控制和收回缺陷药品的能力,只能通过配合单位达成这一目的,因此,笔者倾向于上市许可持有人无需通过自有人力控制和收回缺陷药品。
5.主动召回程序中的主要变化
主动召回程序的变化主要有四点:一是取消了向药监部门提交调查评估报告和召回计划进行备案的要求。二是延长了召回通知的时限要求,现行管理办法规定:“药品生产企业在作出药品召回决定后,应当制定召回计划并组织实施,一级召回在24小时内,二级召回在48小时内,三级召回在72小时内,通知到有关药品经营企业、使用单位停止销售和使用”;征求意见稿规定:“药品上市许可持有人制定召回计划后,一级召回在1日内,二级召回在3日内,三级召回在7日内,通知有关药品生产企业、药品经营企业、医疗机构停止生产、销售和使用。”三是取消了在实施召回的过程中向药监部门报告药品召回进展情况的要求。四是在药品召回后处理措施上,除销毁之外,明确提出了在条件允许情况下可通过“重新标签、修改并完善说明书、重新外包装等”消除药品安全隐患。
6.责令召回程序中的主要变化
责令召回程序的变化主要有两点:一是增加了上市许可持有人根据召回等级时限要求向药监部门提交调查评估报告和召回计划的要求。二是增加了药品上市许可持有人在实施召回的过程中根据召回等级时限要求药监部门报告药品召回进展情况的要求。
7.明确了药品召回信息公开的媒介
现行管理办法中仅规定了药监部门应当“采用有效途径向社会公布存在安全隐患的药品信息和药品召回的情况”,以及规定召回计划中应有“召回信息的公布途径与范围”,对公布途径或媒介并没有指向性或强制性的要求。考虑到药品召回信息本身是不利于所涉药品与企业的负面信息,药企一般本能的不愿意主动公布,笔者曾检索了被药监部门公告药品不符合规定应公布召回信息的药企官网,鲜有药企在自己的官网上公布召回信息。征求意见稿填补了这一空白,明确规定:“药品上市许可持有人应当通过企业官方网站,主动公布存在缺陷的药品信息和召回情况。……没有官方网站的,应在全国性媒体或者所在地省级媒体上发布。”至于上市许可持有人若未按规定在企业官网上发布药品召回信息会承担怎样的法律责任,征求意见稿目前并未明确,《药品管理法》也没有相关规定。同时需注意的是,鉴于一级召回与二级召回的严重性,征求意见稿规定:“实施一级、二级召回的,药品召回信息应当同时申请在所在地省、自治区、直辖市级药品监督部门政务网站发布召回信息。”避免因企业官网受众过少达不到预期公示效果的问题。
8.删除了法律责任一章
征求意见稿在体例上的最大变化是将第五章法律责任全文删除。笔者认为删除这一章有以下三点考虑:一是《药品管理法》对药品全生命周期中各市场主体必要的法律责任已规定的非常详尽,若对市场主体的违法违规行为进行处罚可直接适用。二是对于《药品管理法》未规定的违法情形及法律责任,《药品召回管理办法》作为规章也无权在没有母法依据的情况下设定具体的行政处罚。三是关于药品召回配合单位的相关义务可通过药品上市许可持有人与配合单位签订委托合同进行约定的方式予以解决。







