医疗器械注册人委托生产模式、注册人制度、持有人制度解析
发布时间:2020-07-30
文 | 郭亚飞 合伙人 边不拘 汇业律师事务所
2020年7月7日,国务院发布《关于做好自由贸易试验区第六批改革试点经验复制推广工作的通知》,明确将医疗器械注册人委托生产模式在全国范围内复制推广。这一工作的推进将对我国医疗器械领域业态产生重大影响。本文从基本概念关系、注册人制度发展沿革、该制度与现行规定的区别、现行法规修订评析等方面进行介绍与分析,以便医疗器械领域相关主体在上述推广工作落地前对注册人制度有较为全面的了解。
一、医疗器械注册人委托生产模式、注册人制度、上市许可持有人制度之间的关系
现行《医疗器械生产监督管理办法》(2017年修正)第二十六条规定:“医疗器械委托生产的委托方应当是委托生产医疗器械的境内注册人或者备案人。其中,委托生产不属于按照创新医疗器械特别审批程序审批的境内医疗器械的,委托方应当取得委托生产医疗器械的生产许可或者办理第一类医疗器械生产备案。”
也就是说,绝大多数医疗器械注册申请人在办理了医疗器械注册但没有相应生产许可的情况下,将不可委托生产,只能自行投资生产,不仅重复投入资源,也极大约束了科研成果的产业转化和压制了创新动力。为加快构建开放型经济新体制,优化创新要素的市场配置机制,中央政府决定实施相应改革,对相关市场要素进行必要的“松绑”。
医疗器械“注册人委托生产模式”、“注册人制度”、“上市许可持有人制度”均是在这场医疗器械产业 “松绑”的改革中出现的概念。三者之间联系紧密但存在差异,不少业内人士将之等同看待,存在理解误区。笔者简要厘清如下:
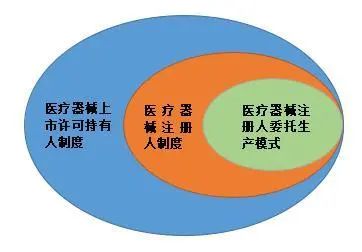
首先,医疗器械“注册人委托生产模式”是“注册人制度”的核心内容。虽然建立新的委托生产模式是释放市场要素的最直接举措,但是生产制造只是医疗器械全生命周期的其中一环,注册人制度还囊括了除此之外关于设计开发、临床试验、销售配送、售后服务、产品召回、不良事件报告等多个环节的职责划分、法律责任承担与监管内容,各环节彼此联结相互作用,其内容远远不限于委托生产。
其次,医疗器械“上市许可持有人制度”包含“注册人制度”。医疗器械实行按照风险程度分类管理。第一类医疗器械实行产品备案管理,第二类、第三类医疗器械实行产品注册管理。从主体上看,司法部2018年6月25日发布的《医疗器械监督管理条例修正案(草案送审稿)》(下称:《修正案草案》)规定:“取得备案凭证或者医疗器械注册证的,为医疗器械上市许可持有人。”可知,医疗器械上市许可持有人包括了第一类医疗器械的备案人与第二、三类医疗器械的注册人,“注册人”仅指第二、三类医疗器械的注册人,因此,医疗器械“上市许可持有人制度”包含“注册人制度”。
三者之间的关系如下图所示:
二、医疗器械注册人制度的发展沿革
基于二、三类医疗器械委托生产的必要性以及相关注册管理体系在医疗器械监管体系中的相对独立性,目前注册人制度正作为重要的改革方向向前推进,其改革的最终目标是在较为成熟的注册人制度基础上建立完整的持有人制度。
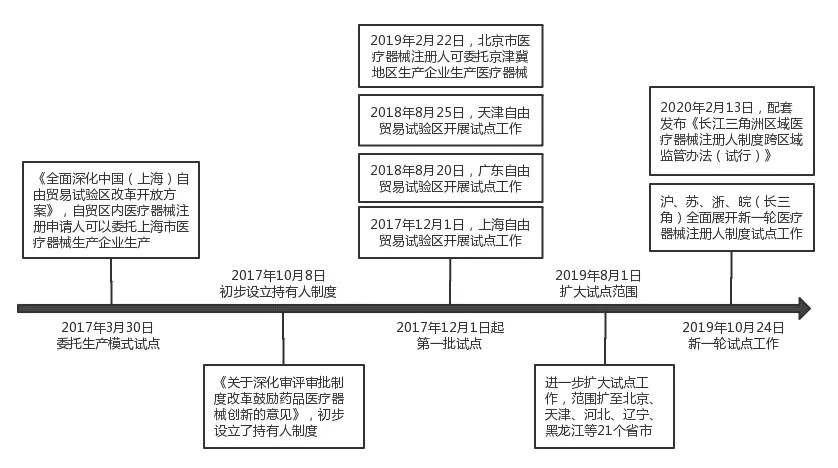
注册人制度发展沿革如下:
2017年3月30日,国务院印发《全面深化中国(上海)自由贸易试验区改革开放方案》,该方案允许自贸试验区内医疗器械注册申请人委托上海市医疗器械生产企业生产产品。
2017年10月8日,中共中央办公厅、国务院办公厅发布《关于深化审评审批制度改革鼓励药品医疗器械创新的意见》(下称:《创新意见》),提出推动上市许可持有人制度全面实施,并首次在国家层面明确了 “医疗器械上市许可持有人”(下称:持有人)的制度概念。《创新意见》允许医疗器械研发机构和科研人员申请医疗器械上市许可,要求持有人须对医疗器械的全生命周期承担全部法律责任,并明确了持有人的受托人在研发、临床试验、生产制造、销售配送环节中的法律责任等,初步设立了持有人制度。
2017年12月1日,上海市食品药品监督管理局(已撤销)印发了关于实施《中国(上海)自由贸易试验区内医疗器械注册人制度试点工作实施方案》(下称:《上海自贸区注册人制度试点方案》)的通知,医疗器械注册人制度由此开始落地试点。2018年8月及2019年1月31日,广东省、天津市、北京市、河北省相继开展医疗器械注册人制度试点工作。
2019年8月1日,为全面实施医疗器械注册人制度进一步积累经验,国家药品监督管理局印发《关于扩大医疗器械注册人制度试点工作的通知》(下称:《扩大注册人制度试点的通知》),将试点扩展至包括现有试点在内的21个省份与直辖市。
2019年10月24日,沪、苏、浙、皖四地共同发布《长江三角洲区域医疗器械注册人制度试点工作实施方案(试行)》,展开跨省际的新一轮医疗器械注册人制度试点工作;2020年2月13日,又配套发布了《长江三角洲区域医疗器械注册人制度跨区域监管办法(试行)》,上述地区注册人制度的试点工作已走在全国前列。
三、试点注册人制度与现行规定的对比
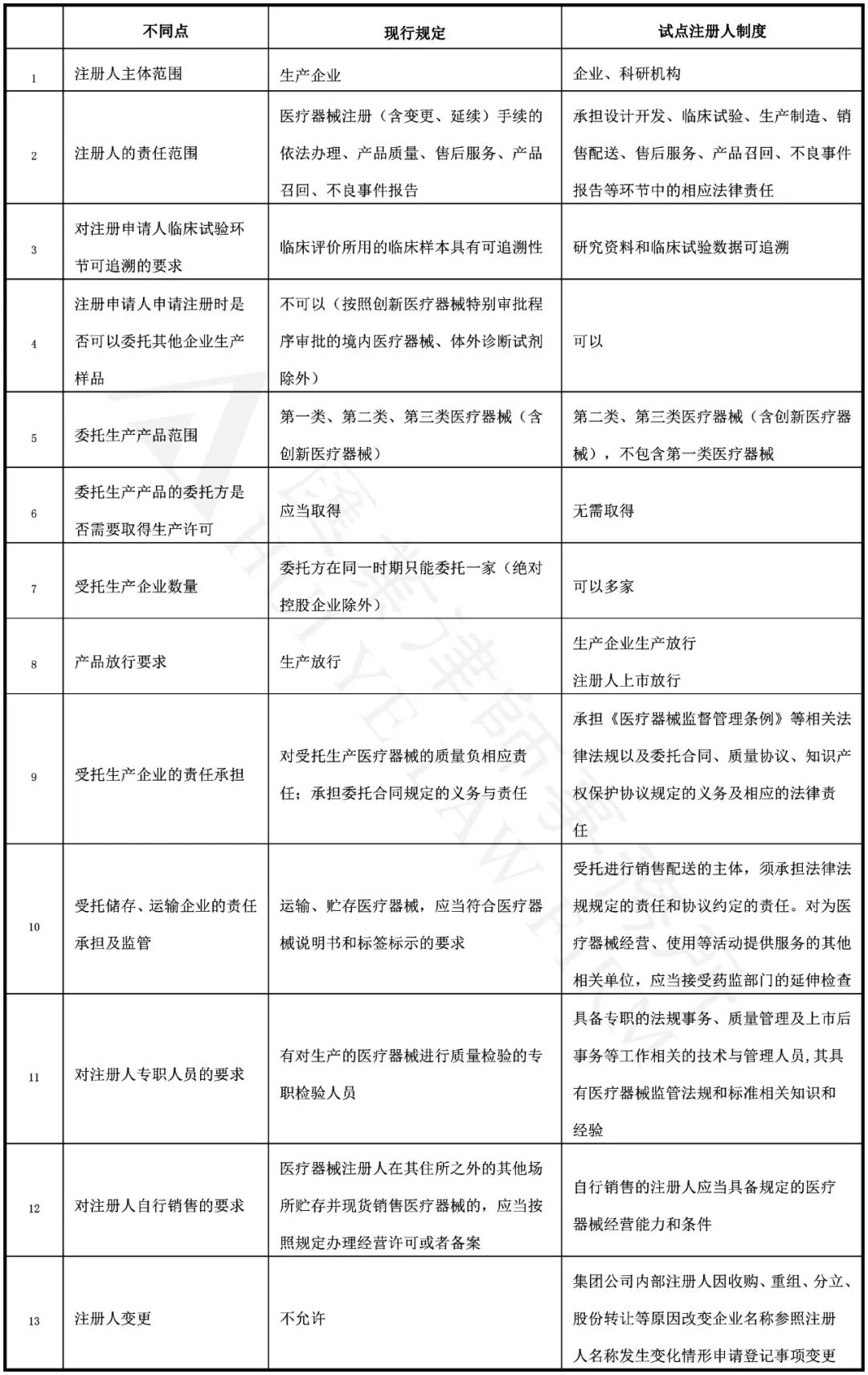
注:
1.现行规定包括:《医疗器械监督管理条例》(2017年修订)、《医疗器械注册管理办法》(2014.10.01生效)、《体外诊断试剂注册管理办法》(2014.10.01生效)、《医疗器械生产监督管理办法》(2017年修正)、医疗器械生产质量管理规范(2015.3.1实施)。
2.注册人制度包括:《创新意见》、《上海自贸区注册人制度试点方案》、《扩大注册人制度试点的通知》、《长江三角洲区域医疗器械注册人制度试点工作实施方案(试行)》。
根据上述制度比照,我们可以看到注册人制度的两个改革方向:
一是尽可能释放市场要素,促进市场资源合理配置。这包括:扩展注册人主体范围、允许注册申请人申请注册时委托生产样品、注册人委托生产产品无需自行具备生产许可、可以多点委托、自行销售未要求办理经营许可、允许集团公司内部注册人变更优化整合资源等。
二是进行责任设计,细化并提升职责要求,为事中事后监管打好基础。体现在:确定注册人的全生命周期法律责任、明确受托生产企业的义务来源以及对注册人提出临床试验研究资料数据可追溯、注册人上市放行、专职法规事务人员配备等深度细化的制度要求等。
由此可以看出,注册人与受托方虽然手脚被“解绑”,但也同时戴上了“紧箍咒”,一旦越线,将随时面临相应监管后果,其势必在医疗器械的全生命周期活动中更为谨慎。
四、《修正案草案》持有人制度评析
如前文所述,从当前改革方向来看,注册人制度是最终建立完整持有人制度的必经之路,持有人制度汲取有益的改革经验已在《修正案草案》中其形初现。因《修正案草案》在现行《医疗器械监督管理条例》基础上修改较多,笔者仅围绕草案中持有人制度相关要点评析如下:
首先,《修正案草案》落实《创新意见》中实施医疗器械上市许可持有人制度的要求,在第二章“医疗器械产品注册与备案”中设专条规定上市许可持有人制度,对持有人及相关受托人的义务作出明确规定(第八条、第十四条),并在相关章节中强化持有人主体责任。但笔者认为,一方面,与正在推进的注册人制度相比,第十四条义务条款并未明确持有人承担自医疗器械设计开发、临床试验开始的全生命周期义务的理念,上市前义务明显弱化。而修正后第七十九条却规定:“医疗器械研制、生产、经营、使用、进出口等活动违反本条例规定的,由医疗器械上市许可持有人承担法律责任”,这一责任条款既缺少研制阶段义务基础的规定,也因为将不良反应、产品召回、再评价责任等规定于其他条款,显得并不完整;另一方面,草案的修改方式相较《药品管理法》中对药品上市许可持有人设置专章而言也明显逊色,持有人相关条款被分散安插于各章节之中缺少系统性,并未充分体现持有人制度在监管体系中的轴心地位。
第二,《修正案草案》增加了境外持有人的代理人的义务条款(第十五条),该条内容与国家市场监督管理总局2018年12月24日公布的《进口医疗器械代理人监督管理办法(征求意见稿)》一致。需要注意的是,两者均规定代理人仅“对产品质量和相关服务违法行为,与境外持有人承担连带责任”,不仅“产品质量和相关服务违法行为”指代不明,也明显侧重于持有人的产品上市后责任。
第三,《修正案草案》在第三章“医疗器械生产”和第四章“医疗器械经营与使用”中,规定了持有人委托生产、销售的权利条款 (第二十七条、第三十五条),明确持有人应当保证质量体系有效运行及提交质量体系自查报告(第二十八条)等,相较试点注册人制度而言,在样品委托生产、是否可多点委托、产品放行等问题上交待不足,但是不排除在现行《医疗器械生产监督管理办法》中进行修订补充的可能。
第四,《修正案草案》增加了持有人从事医疗器械网络销售的规定(第三十八条),这一内容已由生效的《医疗器械网络销售监督管理办法》落实,草案相关内容可能将据此被反向调整。
第五,《修正案草案》在第五章“不良事件的处理与医疗器械的召回”中明确上市许可持有人应当建立医疗器械不良事件监测体系,按规定直接报告医疗器械不良事件(第五十二条),主动开展已上市医疗器械再评价(第五十六条),承担缺陷产品召回的主体责任(第五十七条),基本落实了《创新意见》中产品上市后对注册人的相关要求。
鉴于《修正案草案》推出时注册人制度试点工作起步不久,结合笔者上述分析,可知该版本草案中的持有人制度尚不成熟。2020年07月08日,《国务院办公厅关于印发国务院2020年立法工作计划的通知(国办发〔2020〕18号)》已将《医疗器械监督管理条例(修订)》列入其中,有望在2020年审议通过,笔者将持续关注持有人制度在新修订稿中的修改与完善。







