浅析实验数据在专利申请中的作用
发布时间:2018-08-28
文 | 王函 汇业律师事务所 合伙人
在不同技术领域专利申请中,实验数据所起的作用是不同的。机械、电子、计算机、通信领域的专利申请一般不需要提供实验数据,但如果提供技术效果方面的实验数据,有可能会对后期答复审查意见提供帮助,特别是在创造性评价中实验数据相比简单描述往往会更具说服力。而化学、生物医药领域的专利申请通常要提供实验数据。化学、生物医药领域属于实验学科,与其它技术领域相比存在明显区别,其撰写也存在特殊之处。化学、生物医药发明是否能够实施,往往难以预测,必须借助于实验结果加以证实才能确认。本文将重点对化学、生物医药领域实验数据在专利申请中的作用进行梳理分析。
一、实验数据是化学、生物医药领域专利申请文件的必要组成部分
《专利法》第26条第3款规定:“说明书应当对发明或者实用新型作出清楚、完整的说明,以所属技术领域的技术人员能够实现为准。”《专利审查指南》第二部分第二章中进一步规定:“说明书中给出了具体的技术方案,但未给出实验证据,而该方案又必须依赖实验结果加以证实才能成立。”这种情况属于缺乏解决技术问题的技术手段而被认为无法实现的情形,不符合《专利法》第26条第3款的规定。《专利审查指南》还规定:药物发明必须提供药效实验数据。笔者从化学、生物医药领域专利申请的不同保护客体(产品、用途、制备工艺方法)来分析应如何提供实验数据,见表1。
表1
保护客体 | 新化学或生物产品(例如,化合物、生物制剂等) | 已知化学或生物产品的新用途 | 已知化学或生物产品的新制备工艺方法 |
实验数据 | 证明新化学或生物产品的用途和/或达到预期效果的定性或者定量实验数据 | 证明新用途以及效果的实验数据 | 新工艺所达到更优技术效果的实验数据 |
药效实验数据 | 如果新化学或生物产品是药物,必须提供药效实验数据 | 如果新用途属于医药用途,必须提供药效实验数据 |
二、实验数据可以作为申请文件修改的依据
《专利法》第33条规定:“申请人可以对其专利申请文件进行修改,但是,对发明和实用新型专利申请文件的修改不得超出原说明书和权利要求书记载的范围。”原说明书记载的范围也包括实验数据,因此在撰写申请文件是应当注意,实验数据也可能成为后续审查修改的依据,从而对专利申请的授权前景产生影响。下面笔者通过一个案例来说明实验数据对申请文件修改的作用。
【案例一】

黄芪图片
案情简介:专利申请要求保护一种黄芪提取物在制备防治糖尿病患者对低血糖荷尔蒙反向调节受损的药物中的应用。审查员在实质审查检索中发现了1篇对比文件,对比文件记载“黄芪及其制剂具有双向调节血糖的作用,黄芪注射液具有治疗糖尿病肾病的作用”。审查员认为,本领域技术人员知道“防治糖尿病患者对低血糖荷尔蒙反向调节受损的药物”实质上是一种针对血糖过低患者升高血糖的药物,其适应症应是低血糖。本领域技术人员根据对比文件1指出的“黄芪及其制剂具有双向调节血糖的作用”有启示认为黄芪注射液具有升高血糖的作用,是显而易见的,不具备创造性。申请人在答复时将权利要求1修改为“一种黄芪提取物在制备治疗糖尿病并发症HAAF的药物中的应用”,修改依据为说明书中的相关实验数据,从实验数据可见,黄芪的作用是对大鼠荷尔蒙的重建,从而增强其对低血糖的交感神经系统的反应,起到一种预警机制,而并非是审查员认为的黄芪提取物起到“升高血糖”的作用。修改后的权利要求1明确记载了本发明黄芪提取物的适应症是“糖尿病并发症HAAF(即低血糖相关的自主神经系统调节失败)”,其适应症并非是审查员所认为的“低血糖”。对比文件记载的“黄芪及其制剂具有双向调节血糖的作用”与本发明权利要求1要求保护的新用途“治疗糖尿病并发症HAAF(低血糖相关的自主神经系统调节失败)”存在本质上的区别,从而说明本申请相对于对比文件具备创造性。最终审查员接受了申请人陈述的理由,该申请最终被授予专利权。
基于上述案例分析可知,实验数据作为申请文件的组成部分,可以作为申请文件的修改依据,从而对专利申请的最终授权前景起重要作用。
三、实验数据在创造性评价中起关键作用
在化学、生物医药领域专利申请中,审查员在创造性评价中往往要求技术方案达到预料不到的技术效果,而预料不到的技术效果往往必须通过对比实验数据来证明。
《专利审查指南》第二部分第十章规定:“结构上与已知化学、生物医药产品接近的产品,必须要有预料不到的用途或者效果,才具备创造性;已知产品用途发明,要求该新用途不能从产品本身的结构、组成、分子量、已知的物理化学性质以及该产品的现有用途显而易见地得出或者预见到,而是利用了产品新发现的性质,并且产生了预料不到的技术效果,才具备创造性。”
在实际操作中,发明人提供的技术交底书中往往记载的仅仅是最佳的实验数据,而非对比实验数据。没有经验的专利代理人可能会直接把该最佳实验数据放到说明书中,这样的做法存在如下风险:
1.最终授权的权利要求保护范围很可能限缩到该最佳实施例,保护范围很窄,竞争对手可以轻易绕开、规避该专利,起不到真正的保护作用。
2.影响审查员的创造性判断,导致最终专利申请无法获得授权。例如,生物检测试剂盒领域,关于引物和探针的设计,由于引物和探针的设计方法属于本领域的常规方法,针对特定的基因设计引物和探针是本领域技术人员很容易做到的,如果在专利申请文件中仅记载要求保护的最佳引物和探针的实验数据,那么审查员通常会以不具备创造性驳回该专利申请。经验丰富的专利律师会提醒发明人,要求补充筛选最佳引物的对比实验数据,筛选过程的对比实验数据可以体现创造性劳动,要特别注意的是,多对引物和探针的对比实验数据证明的最佳引物的技术效果应该能达到其它引物所预料不到的技术效果,才能证明其具备创造性。
根据《国家知识产权局关于修改〈专利审查指南〉的决定》(第七十四号国家知识产权局令),2017年4月1日起施行的《专利审查指南》第二部分第十章第3节中新增“3.5 关于补交的实验数据”一节,规定:“对于申请日之后补交的实验数据,审查员应当予以审查。补交实验数据所证明的技术效果应当是所属技术领域的技术人员能够从专利申请公开的内容中得到的”。下面笔者再通过一个案例来探讨申请日后补交实验数据的审查标准。
【案例二】
案情简介:针对请求人戴锦良就专利权人瑞士诺华公司(下称诺华公司)的发明专利(专利号:ZL201110029600.7)提出的无效宣告请求案,国家知识产权局专利复审委员会(下称专利复审委员会)经审理后作出无效宣告请求审查决定,宣告专利权全部无效。在上述无效宣告请求案中,双方当事人的争议焦点之一在于能否接受申请日后补交的实验数据以证明发明取得了预料不到的技术效果。在“含有缬沙坦和NEP抑制剂的药物组合物”专利权无效宣告请求案中,涉案专利是一种包含缬沙坦和沙库巴曲的药物组合物。无效宣告请求人认为:最接近的现有技术已经公开了NEP抑制剂和血管紧张素Ⅱ受体拮抗剂的组合物,用于治疗高血压和充血性心力衰竭,另有证据表明,沙库巴曲是已知的NEP抑制剂,缬沙坦是已知的血管紧张素Ⅱ受体拮抗剂,且二者均具有降血压的作用,本专利声称药物组合物之间存在协同作用,但是该效果不能被证实,因此,权利要求1不具备创造性。在该案的审理过程中,专利权人提交了发明人作出的声明(下称反证1),用于证明缬沙坦和沙库巴曲的药物组合物在高血压动物模型中具有降低平均动脉压的协同作用。反证1属于申请日后补交的实验数据,所证明的技术效果是否属于本技术领域的技术人员能够从专利申请公开的内容中得到的,应结合本领域的普通技术知识和专利申请公开的内容进行具体分析综合判断。
涉案专利附图:

怎样的技术效果才是本技术领域的技术人员能够从专利申请公开的内容中得到的技术效果?笔者认为:专利申请文件证实的技术效果毫无疑问属于本技术领域的技术人员能够从专利申请公开的内容中得到的技术效果。而没有被专利申请文件证实的技术效果可以分为两类,一类是所属领域技术人员能够预期的技术效果,另一类是所属领域技术人员预料不到的技术效果。

缬沙坦和沙库巴曲均是已知具有降血压作用的化合物,二者组合之后,在没有反证的情况下,即使说明书没有提供实验数据,所属领域技术人员也能得到二者组合后仍然能够发挥一定的降血压作用,这属于能够预期的技术效果。而缬沙坦和沙库巴曲组成的组合物在降血压方面具有协同作用是所属领域技术人员的认知水平不能预期的效果,属于预料不到的技术效果。药物发明的预料不到的技术效果依赖实验证实,因此,申请人撰写药物发明专利申请文件时,对于所属领域技术人员不能确认的效果或用途,应在说明书中提供充足的药效实验资料以证实该技术效果。组合物具有协同作用的实验数据在申请日后补交一般不予接受,笔者建议在原始申请文件中提供组合物具有协同作用的实验数据。
笔者认为,证明预料不到技术效果的实验数据在申请日后补交一般不予接受,建议发明人在原始申请文件中记载。那么,哪些情况下原始申请文件需要记载预料不到技术效果的实验数据呢?下面笔者列举了一些情况,供大家参考:
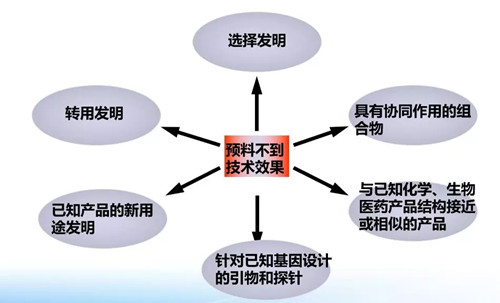
选择发明,是指从现有技术中公开的宽范围中,有目的地选出现有技术中未提到的窄范围或个体的发明。
转用发明,是指将某一技术领域的现有技术转用到其他技术领域中的发明。
根据笔者在实务中积累的经验,补交实验数据证明的技术效果应该是说明书中有实验数据或其它证据支持的,仅仅在说明书中存在简单表述而没有任何实验数据或证据支持,之后在答复过程中补交数据,审查员一般是不会予以考虑的。通常审查员予以接受补交实验数据的情况是:原始申请文件中对本发明的某项技术效果记载了相关实验数据,申请人补充了对比文件作为对照组与本发明中记载的该技术效果数据进行对比,对比的前提是对照组采用的实验条件和实验步骤应当与原始申请文件中记载的相关实验一致。笔者建议发明人在申请专利时委托有经验的专利律师精心策划、充分检索,做好战略布局,设计好相应的实验方案和对比实验来证明技术效果,以提高专利授权前景和专利稳定性,才能获得高质量、高价值的专利,提升企业的核心竞争力。
四、有关专利申请实验数据的七问七答
在实务中,经常有客户咨询有关专利申请实验数据的问题,笔者总结了以下常见问题与答案,供大家参考。
1.专利申请必须要提供实验数据吗?
答:机械、电子、计算机、通信领域的专利申请一般不需要提供实验数据。化学、生物医药领域的专利申请通常要提供能证明产品用途以及效果的实验数据。
2.药物专利申请要求提供的药效实验数据必须是临床实验数据吗?
答:药效实验数据可以是临床实验数据,也可以是动物实验数据,甚至是细胞实验数据都可以,只要证明有相应的治疗效果即可,不是一定要等到临床实验数据出来才能申请专利,通常只要有动物实验数据(甚至是细胞实验数据)就可以申请专利。
3.专利申请中的实验数据以什么形式表达,需要具体到何种程度?
答:实验数据可以以表格、图的形式表达,图不能是彩色图,必须提供黑白图。在提供实验数据时,应当给出必要的实验条件和方法。
4.专利申请中对实验数据采用的样本数量有规定吗?
答:对于实验数据采用的样本数量在专利申请文件中没有要求,专利申请中的实验数据的要求相比学术论文要低很多,原则上只要实验数据能证明产品用途以及效果即可。
5.专利审查指南规定的对于申请日之后补交的实验数据,可以直接补充到申请文件中吗?
答:《专利审查指南》规定的对于申请日之后补交的实验数据,不能直接补充到申请文件中,不符合《专利法》第33条的规定:“申请人可以对其专利申请文件进行修改,但是,对发明和实用新型专利申请文件的修改不得超出原说明书和权利要求书记载的范围”。但是,申请日之后补交的实验数据,可以作为申请人意见陈述创造性理由的相关证据,审查员应当予以审查。
6.《专利审查指南》规定的对于申请日之后补交的实验数据,是指在专利申请日之后的所有审查程序中都可以补交实验数据吗?
答:《专利审查指南》规定的对于申请日之后补交的实验数据,通常在如下时间可以补交实验数据:实质审查中申请人答复审查意见通知意见陈述时;复审程序中提交复审请求书时或答复复审通知书意见陈述时;无效程序中专利权人提交反证时。
7.在专利申请后能不能补充实验数据到原始申请文件中?
答:在专利申请后补充实验数据到原始申请文件中,不符合《专利法》第33条规定,一般不予接受。但在以下情况可以补充实验数据:即以在先申请为优先权基础,补充实验数据递交新的专利申请,这种情况往往发生在申请人由于种种原因需要尽快拿到专利申请号,确定申请日,在实验数据不完善的情况下,可以先递交申请,然后利用1年的优先权期限,在1年内补充实验数据重新递交申请。







